健康知识库
TIL免疫疗法!
编辑:ddayh.cn
- 上一篇:肺癌脑转移虽然凶险但我们有秘密武器!
- 下一篇:胆道恶性肿瘤的靶向及免疫治疗!
- 200乳腺癌内分泌治疗
- 200副作用治疗
- 200胃癌患者术后注意事项
- 2002017年肺癌TNM分期
- 200非小细胞肺癌的四代EGFR-TKI靶向
- 200史上最全靶向治疗及免疫治疗大盘
- 200免疫治疗最全、最实用科普!
- 200肿瘤科普文章系列一:三分钟带你
- 200T-spot结核鉴别
- 200食品、补品或药品,都要一个度~
- 200癌症筛查怎么做
- 200每个人体内都有原癌基因和抑癌基
- 200乳腺的一生原来是这个样子的……
- 200你可能误会肿瘤了
- 200血友病是一种遗传性的,由于凝血
- 200腋下淋巴癌早期症状
- 200胃良性肿瘤如何鉴别诊断
- 200怎么样自我检查口腔癌
- 200产后得宫颈癌的原因有哪些
- 200胃窦癌症状和治疗方法
邱立新,就职于复旦大学附属肿瘤医院肿瘤内科。主要从事胃癌、肠癌等恶性肿瘤的化疗、靶向治疗、免疫治疗和研究。创办了肿瘤科普公众号“邱立新医生(qiulixinyisheng)”。
在International? Journal of Cancer、European Journal of Cancer等发表SCI论文65篇,累计影响因子约300 分,其中第一或并列第一作者SCI论文40篇,累计影响 因子约180分。副主编《赢在论文*术篇》、参编《实用循证医学方法学》。负责国家自然科学基金、中国临床肿瘤学科学基金等。获得教育部科技进步二等奖、上海市医学科技进步奖三等奖、上海医学院首届青年学者论坛二等奖等 。
目前肿瘤免疫治疗可以分为两大类:
一类是免疫检查点抗体类药物,用于解除肿瘤微环境对免疫的耐受和屏蔽作用,阻断被屏蔽的免疫信号,让免疫细胞保持对肿瘤产生攻击的能力,治疗方法多为针对PD-1、PD-L1、CTLA-4等靶点的小分子药物和抗体药物。
二是过继T细胞疗法(adoptive T-cell therapy,ACT),也就是我们常说的免疫细胞治疗,治疗方法除了早期的LAK,DC,CIK,DC-CIK之外,近年来的CAR-T,TCR-T,TIL(肿瘤浸润性淋巴细胞)等疗法在不同层面上解决了T细胞对肿瘤的识别性难题,逐渐在临床试验中体现出优异的疗效。
一、什么是TIL细胞?
TIL(Tumor Infiltrating Lymphocytes,肿瘤浸润淋巴细胞)是一种从肿瘤组织中分离出的浸润淋巴细胞。这些淋巴细胞中有部分是针对肿瘤特异性突变抗原的T细胞,是深入到敌军内部打击能力最强的免疫细胞,被认为是一种机体对肿瘤细胞特异性免疫反应。
![]()
![]() ????????????
????????????
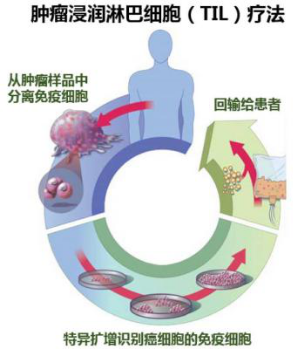
二、什么是TIL细胞疗法?
TIL细胞疗法是指从肿瘤组织中分离肿瘤浸润的淋巴细胞,在体外培养和大量扩增后回输到病人体内的疗法。TIL疗法的效应细胞是经过天然选择与富集,肿瘤特异性T细胞比例高且多样性丰富的群体,与CAR-T细胞疗法和PD-1/PD-L1抗体相比,具有多靶点、肿瘤趋向和浸润能力强、副作用小等优点。
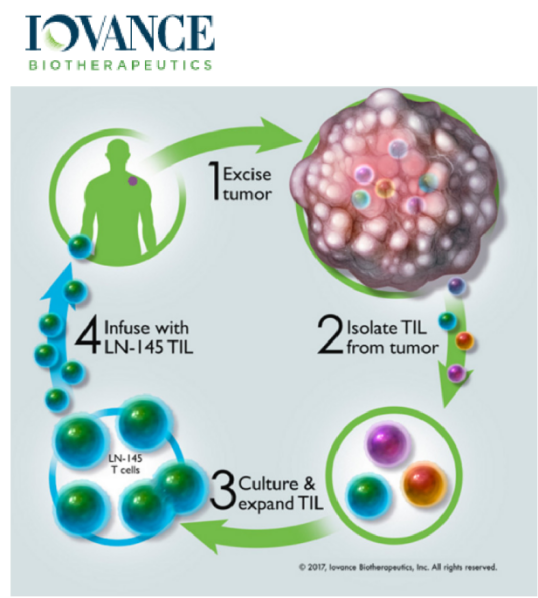
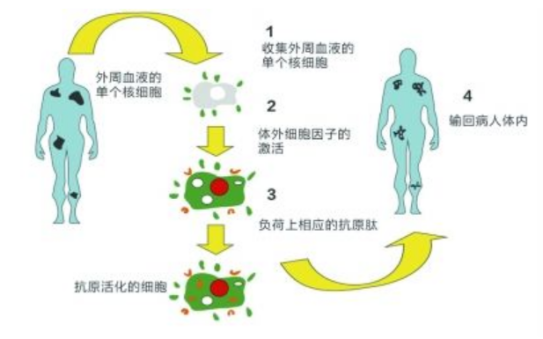
三、TIL免疫疗法的具体步骤与流程是什么呢?
1. 我们得到病人的肿瘤组织块,其中混杂着体积较大的肿瘤细胞以及体积小而圆的T淋巴细胞;
2. 肿瘤样本被运送到专有的GMP设施,在那里TIL被分离并繁殖,将不同种类的T淋巴细胞在细胞板上克隆化,并加入高浓度的IL-2来选择培养,在三周内产生数十亿TIL。
3. 在IL-2的刺激下不同种类的T淋巴细胞都得到了克隆扩增,形成了细胞群;
4. 用病人的肿瘤细胞和扩增后的T淋巴细胞反应,凡是能够发生杀瘤效应的T淋巴细胞群作为阳性TIL群留下,其余的丢弃;
5. 用负载了肿瘤特异性抗原的树突状细胞(DC)进一步扩增培养肿瘤特异性的TIL;
6. 患者开始一周的预处理治疗(清髓)以准备接受TIL。TIL产品作为一次性疗法使用,在TIL输注后立即接受多达6剂白细胞介素2(IL-2),来支持患者体内TIL的生长和激活。
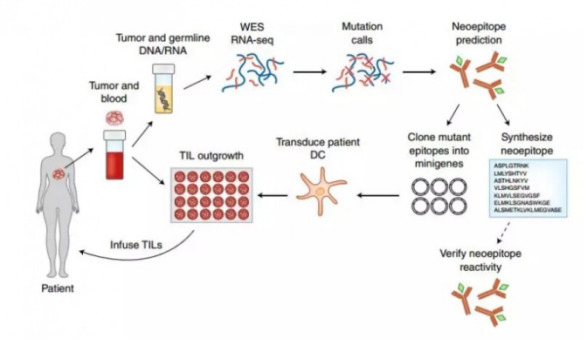
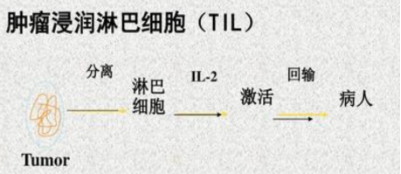
四、TIL细胞与其他细胞的不同
1.LAK、CD3AK、DC、CIK、NK等免疫细胞,均来自外周血,靶向性弱。
2.TIL细胞来自于肿瘤组织内部,有60%以上能识别肿瘤细胞,有很强的靶向性。
3.TIL细胞杀伤力高,比LAK强50-100倍。
4.宿主处于免疫抑制状态,反而有利于增强TIL的杀伤作用,适合与放化疗联用。
5.TIL细胞的扩增能力比LAK细胞强。
6.采用定向筛选技术后,TIL的疗效显著增强,且通常只需要注射一次。

五、TIL和老一代细胞免疫疗法的不同
乍一看,TIL疗法和魏则西用过被国家叫停的CIK疗法很像,这两者有何区别?
它们都属于细胞免疫疗法,基本都是从患者身上提取免疫细胞,体外扩增,然后输回去。
但TIL和老一代细胞免疫疗法,比如CIK,有两个非常重要的区别:
1.?1.?免疫细胞来源不同,TIL的免疫细胞来自于肿瘤组织,而CIK来自血液。
肿瘤里分离出的免疫细胞,有60%以上能识别肿瘤,而血液里面分离的免疫细胞,这个比例不到0.5%。不能识别癌细胞的免疫细胞,对患者来说没用。
相比从血液里面分离细胞,提取新鲜肿瘤组织,从中分离TIL在技术上难很多,也是为啥很多人明知TIL更好,却还持之以恒推销CIK的原因。
2.?新一代TIL疗法增加了定向筛选过程,确保只扩增识别肿瘤细胞的免疫细胞。
TIL不仅分离出的免疫细胞更对口,而且扩增的时候会再筛选,确保只留下针对癌症的免疫细胞。
以上两点区别,造成TIL疗法中输回的是大量专门针对癌细胞的免疫细胞,而CIK输回的细胞虽然也不少,但多数是打酱油的。
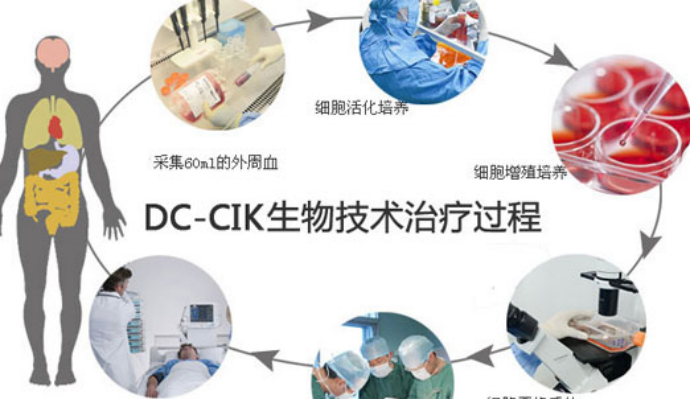
六、TIL细胞疗法与其它新的免疫疗法的不同
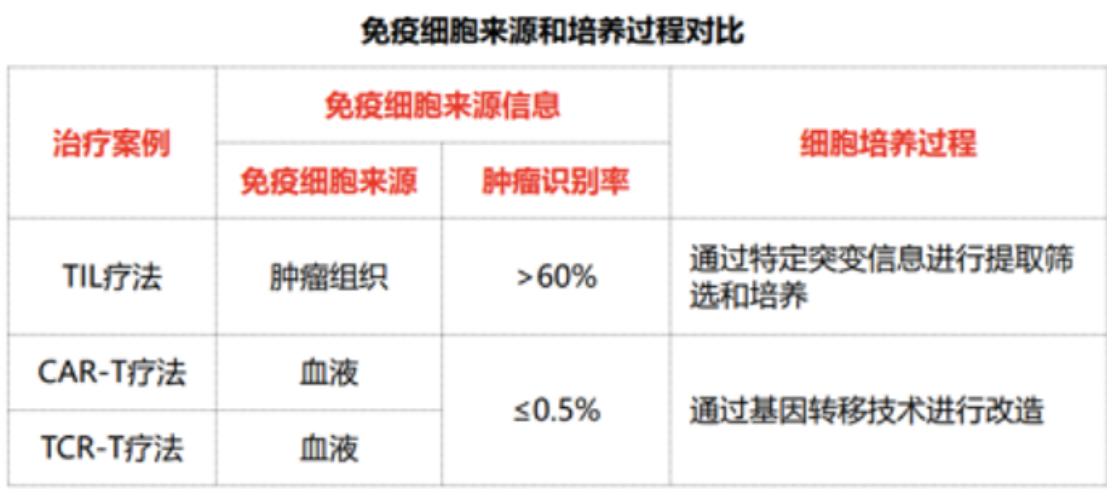
1.?CAR-T:CAR-T细胞疗法是指将经过设计的CAR-T细胞可在实验室培养生长,达到数十亿之多将扩增后的CAR-T细胞注入到患者体内,注入之后的T细胞也会在患者体内增殖,并杀死具有相应特异性抗原的肿瘤细胞。CAR是一种蛋白质受体,可使T细胞识别肿瘤细胞表面的特定蛋白质(抗原),表达CAR的T细胞可识别并结合肿瘤抗原,进而攻击肿瘤细胞。这种表达CAR的T细胞被称为CAR-T。CAR-T对白血病和B细胞淋巴瘤的效果好,对实体瘤的效果不尽如意,主要是缺少理想的靶标。理想的目标抗原是仅在肿瘤细胞表面表达的肿瘤特异性抗原。不幸的是肿瘤表达的大多数抗原不具备肿瘤特异,因此大多数的CAR都以肿瘤相关性抗原作为靶点,但这往往会导致“脱靶”的可能性。2.?TCR疗法:T细胞受体(TCR)是指,将患者体内的普通T细胞分离出来,利用基因工程技术引入新的基因,使转基因T细胞表达能够识别癌细胞的TCR,回输到患者体内从而杀死肿瘤细胞的治疗方法。TCR的作用机制是向普通T细胞中引入新的基因,使得新的T细胞能够表达TCR从而有效识别肿瘤细胞,引导T细胞杀死肿瘤细胞。TCR能靶向源自突变的肿瘤新生抗原,肿瘤新生抗原对肿瘤本身具有非常特异性的优势,减轻了脱靶识别的危险。但是TCR工程改造存在一定的问题。首先,T细胞内源性的TCR仍然存在,抑制了表面表达和产生错配假体TCR,导致转基因TCR功能的下降,有可能导致自身反应或/和移植物抗宿主病(GVHD)。其次,病毒转导会导致转基因随机整合,非病毒转导例如“睡美人” 转座系统也会存在至少半随机基因整合,带来安全性问题。
3.?TIL疗法与CAR-T和TCR细胞疗法的区别在于,T细胞不需要经过基因工程的改造。TIL疗法由靶向癌细胞中多种抗原的T细胞组成,因此可以通过多个靶点激发对癌细胞的细胞毒性反应。而CAR-T和TCR细胞疗法通常只能靶向一个抗原,这让癌细胞可能更容易对它们产生抗性。目前,TCR和CAR-T疗法在治疗实体瘤方面进展有限,而TIL疗法已经在多种癌症类型中产生了可喜的疗效。
七、?TIL免疫疗法的优势
1.?针对性地杀死癌细胞
利用肿瘤杀伤性TIL淋巴细胞进行癌症免疫治疗具有特异性,针对性杀死癌细胞,肿瘤病灶明显缩小。定向筛选过程,确保只扩增识别肿瘤细胞的免疫细胞。
2.?抗复发性强
抗复发性强,对于手术后残存肿瘤细胞的清除,对于手术后抗复发性与转移治疗,配合放化疗更有显著疗效。
3.?适应多种实体肿瘤
?适应症广,对原发肿瘤、转移灶均有明显疗效。体外实验后回输,安全性高,回输次数少,副作用小。
胃癌 肺癌 肝癌 乳腺癌 肾癌 食道癌 子宫颈癌 胆管癌 卵巢癌 脑瘤 黑色素瘤
4.?强强联合,杀癌效果倍增!
这些免疫细胞经过体外培养后,重新注入到患者体内。同时,研究团队联合使用了免疫增强药物白细胞介素2和另一种“明星抗癌药”PD-1抑制剂Keytruda,Keytruda即属于另一种免疫疗法免疫检查点阻断,在某些癌症中有显著的效果。现在,大量的研究已经证实肿瘤细胞会通过产生一些逃蛋白来伪装自己,如PD-L1和CTLA-4刹车分子,抑制免疫细胞的反应。因此,很多科学家对于TIL疗法和PD-1抗体的“双剑合璧”充满期待:PD-1/PD-L1抗体可以解除免疫抑制,让回输的TIL细胞更加“愉快”的杀死癌细胞。
八、TIL免疫疗法的局限性
作为一种高度差异化、定制化和靶向性的免疫疗法,TIL疗法在有效性、安全性和可及性方面仍存在一定的局限性:
1.?能提取淋巴细胞的新鲜肿瘤样本难获得(一般只能通过手术获取,需要医院/手术医生的全力配合)
2.?具有抗肿瘤活性、增殖能力强的TIL细胞难获得(除了后期的体外筛选和扩增,也取决于肿瘤周围是否有比较多的T细胞浸润)
3.?TIL会被肿瘤微环境抑制
4.?无法保证回输的T细胞在体内能存足够的时间
5.?涉及多种系统用药、回输后副反应的管理
6.?TIL细胞的体外扩增缺乏标准流程,现有操作程序成本高、耗时长
九、临床案例
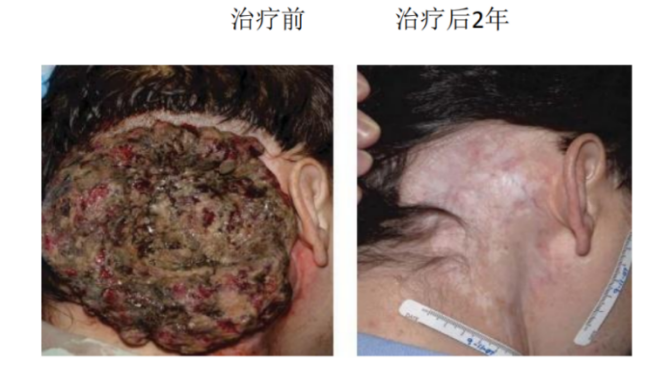
1.?黑色素瘤
一项LN-144治疗转移性黑色素瘤的II期的临床试验,入组的转移性黑色素瘤患者必须接受至少一次全身治疗,这其中包括免疫检查点抑制剂,也包括BRAF抑制剂。一共62名患者疗效可评价。
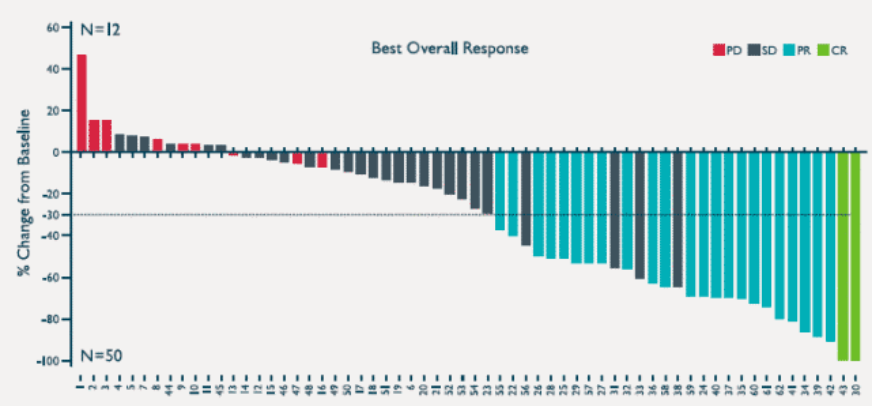
结果显示:LN-144治疗的客观缓解率(ORR)为38%,疾病控制率(DCR)为80%,其中2名患者完全缓解,23名患者部分缓解。
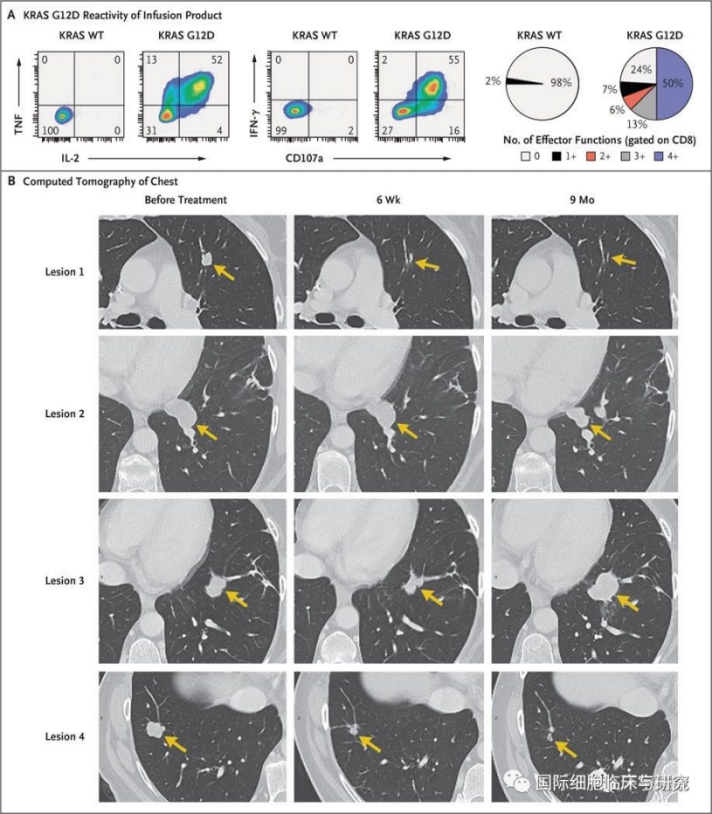
2.?晚期结直肠癌
??在2016年发表的文献中,一名转移性结直肠癌患者接受了靶向KRAS G12D突变的TIL治疗后,患者肺部的7个转移灶中有6个明显缩小,其中3个完全消失。患者在4年后仍然没有疾病进展。
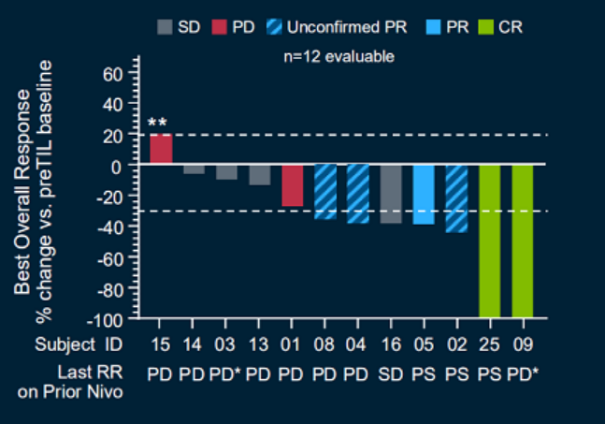
3.?晚期肺癌
?肺癌是全球发病和死亡最高的癌症,尽管近年来靶向和免疫治疗发展已经让肺癌越来越趋于慢性病的治疗,但是对于一些患者来说,当最后的保底药物PD-1发生耐药后,仍让患者们感到恐慌。
??这项试验共有32名患者参加,最终有16名患者接受TILS治疗,其中12名患者可以评估。在平均随访1.4年时,3名患者病情缓解,其中两名完全患者,并且已超过一年。另一名患者的缓解即将得到确认。
4.?晚期宫颈癌
?一项LN-145用于晚期宫颈癌的II期临床试验,数据最亮眼。这项临床试验入组的大多为二至三种治疗失败的晚期宫颈癌患者,属于难治性病例,一共27名患者疗效可评价。
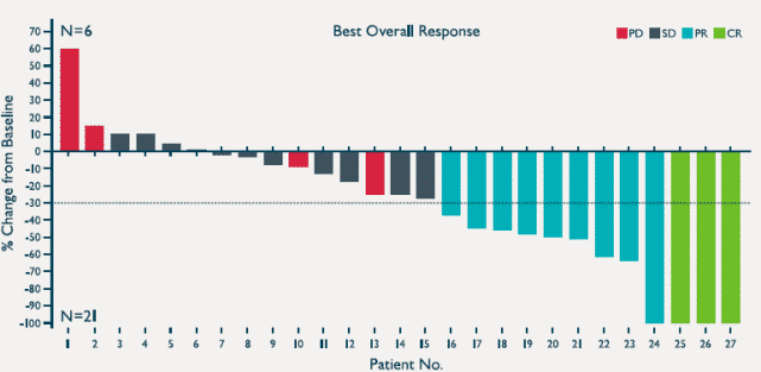
结果显示:中位随访时间3.5个月时,LN-145治疗的客观缓解率(ORR)为44%,疾病控制率(DCR)为85%,其中3名患者肿瘤完全消失,9名患者肿瘤明显缩小。
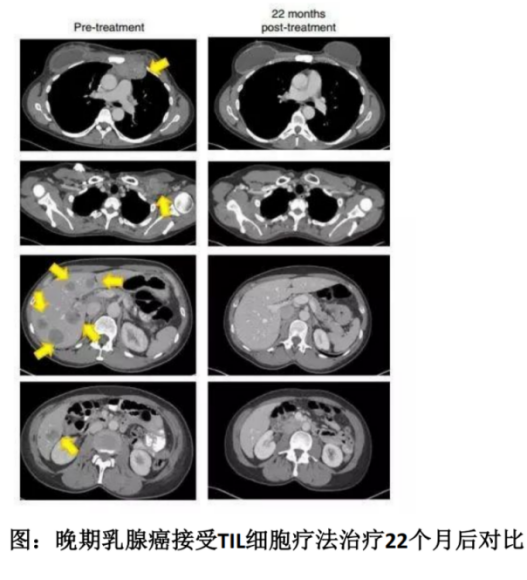
5.?转移性乳腺癌
一名难治性激素阳性转移性乳腺癌患者接受了4种突变蛋白(SLC3A2,KIAA0368,CADPS2和CTSB)的TILs,治疗22个月后,患者肿瘤完全消失,且4年后仍未出现进展或复发。这一案例发表在2018年《自然医学》(Nature Medicine)杂志上。
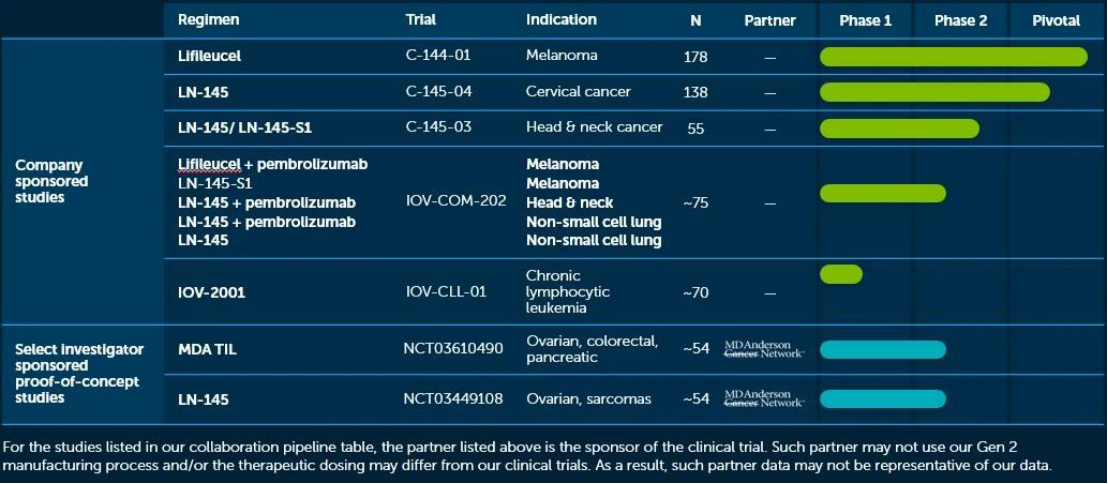
十、相关临床试验
目前,这款新型的免疫疗法暂未上市,但在全球范围内开展了多项针对各类实体肿瘤(非小细胞肺癌,结直肠癌,卵巢癌,黑色素瘤...)的临床试验。
?目前,美国的TILs治疗技术只能通过新鲜肿瘤组织提取TILs细胞,因此,肿瘤患者在手术后第一时间将肿瘤组织中杀癌能力最强的这部分TILs细胞储存起来,在手术后或癌症复发时扩增回输到体内,这将是战胜癌症最宝贵的机会之一。国内的TILs技术在此基础上进行了调整,可通过血液或抽取胸腹水提取。目前美国和国内的TILs疗法均未正式上市,只能通过临床试验接受治疗,大家需要慎重选择。我们期待这款新型免疫疗法能够早日获批上市,给肿瘤患者带来新的治疗选择。
我们有信心战胜肿瘤,滚蛋吧――肿瘤君!
微信扫描下方二维码皆可咨询TIL细胞免疫治疗,能帮到您是我最大的荣幸~

更多文章点击这里
EGFR靶点介绍、相关治疗药物及临床研究
ALK靶点介绍、相关治疗药物及临床研究
ROS1靶点介绍、相关治疗药物及临床研究
MET靶点介绍、相关治疗药物及临床研究
HER2靶点介绍、相关治疗药物及临床研究
BRAF靶点介绍、相关治疗药物及临床研究
BRCA靶点介绍、相关治疗药物及临床研究
MSI相关介绍、治疗药物及临床研究
免疫治疗最全、最实用科普
免疫治疗的十万个为什么
免疫治疗太贵,怎么办?
热门肿瘤外科